의약품 제조업체: Novartis Pharmaceuticals Corporation (Updated: 2024-07-18)
처방 정보의 주요 내용
ZYKADIA® (세리티닙) 캡슐, 경구용
ZYKADIA® (세리티닙) 정제, 경구용
미국 최초 승인: 2014
최근 주요 변경 사항
| 경고 및 주의 사항, 위장관계 부작용 (5.1) | 8/2021 |
적응증 및 사용법
투여량 및 투여 방법
권장 투여량: 음식과 함께 하루에 한 번 경구로 450mg. (2.2)
금기 사항
없음. (4)
경고 및 주의 사항
- 위장관계 부작용: ZYKADIA는 위장관계 부작용을 유발할 수 있습니다. 심각하거나 참을 수 없을 경우, 구토 방지제 또는 설사 방지제에 반응하지 않으면 투여를 중단합니다. 호전되면 ZYKADIA를 감량하여 재개합니다. (2.3, 5.1)
- 간 독성: ZYKADIA는 간 독성을 유발할 수 있습니다. 최소한 매월 간 기능 검사를 모니터링합니다. 투여를 중단한 다음 감량하거나 ZYKADIA를 영구적으로 중단합니다. (2.3, 5.2)
- 간질성 폐 질환/폐렴: 환자의 2.4%에서 발생했습니다. 치료 관련 간질성 폐 질환(ILD)/폐렴이 진단된 환자에게는 ZYKADIA를 영구적으로 중단합니다. (2.3, 5.3)
- QT 간격 연장: ZYKADIA는 QTc 간격 연장을 유발할 수 있습니다. 울혈성 심부전, 서맥성 부정맥, 전해질 이상이 있는 환자 또는 QTc 간격 연장을 유발하는 것으로 알려진 약물을 복용하는 환자의 심전도 및 전해질을 모니터링합니다. 투여를 중단한 다음 감량하거나 ZYKADIA를 영구적으로 중단합니다. (2.3, 5.4)
- 고혈당: ZYKADIA는 고혈당을 유발할 수 있습니다. 치료 전에 공복 혈당을 모니터링하고 그 후 주기적으로 모니터링합니다. 필요에 따라 항고혈당제를 시작하거나 최적화합니다. 투여를 중단한 다음 감량하거나 ZYKADIA를 영구적으로 중단합니다. (2.3, 5.5)
- 서맥: ZYKADIA는 서맥을 유발할 수 있습니다. 심박수와 혈압을 정기적으로 모니터링합니다. 투여를 중단한 다음 감량하거나 ZYKADIA를 영구적으로 중단합니다. (2.3, 5.6)
- 췌장염: 리파아제 및/또는 아밀라아제 수치 상승 및 췌장염이 발생할 수 있습니다. 임상적으로 필요에 따라 치료 전에 리파아제와 아밀라아제를 모니터링하고 그 후 주기적으로 모니터링합니다. 투여를 중단한 다음 ZYKADIA를 감량합니다. (2.3, 5.7)
- 태아 독성: ZYKADIA는 태아에게 해를 끼칠 수 있습니다. 임신 가능성이 있는 여성에게 태아에 대한 잠재적 위험을 알리고 효과적인 피임법을 사용하도록 조언합니다. (5.8, 8.1, 8.3)
부작용
ZYKADIA 450mg를 음식과 함께 복용한 환자에서 가장 흔한 부작용(발생률 ≥ 25%)은 설사, 메스꺼움, 복통, 구토 및 피로이며, ZYKADIA 750mg을 공복 상태에서 복용한 환자에서 가장 흔한 부작용은 설사, 메스꺼움, 구토, 피로, 복통, 식욕 감소 및 체중 감소입니다. (6)
의심되는 부작용을 보고하려면 Novartis Pharmaceuticals Corporation에 1-888-669-6682 또는 FDA에 1-800-FDA-1088 또는 www.fda.gov/medwatch로 연락하십시오.
약물 상호 작용
특정 인구 집단에서의 사용
환자 상담 정보 및 FDA 승인 환자 라벨은 17을 참조하십시오.
개정: 10/2021
목차
전문 정보: 목차*
1
적응증 및 사용법
2
투여량 및 투여 방법
2.1
환자 선택
2.2
권장 용량
2.3
부작용에 대한 용량 조절
2.4
강력한 CYP3A 억제제에 대한 용량 조절
2.5
중증 간 기능 장애 환자에 대한 용량 조절
3
제형 및 강도
4
금기 사항
5
경고 및 주의 사항
5.1
위장관 부작용
5.2
간 독성
5.3
간질성 폐 질환/폐렴
5.4
QT 간격 연장
5.5
고혈당증
5.6
서맥
5.7
췌장염
5.8
태아 독성
6
부작용
6.1
임상 시험 경험
7
약물 상호 작용
7.1
다른 약물의 ZYKADIA에 대한 영향
7.2
ZYKADIA의 다른 약물에 대한 영향
7.3
QT 간격을 연장하는 약물
7.4
서맥을 유발하는 약물
8
특정 집단에서의 사용
8.1
임신
8.2
수유
8.3
생식 능력이 있는 여성 및 남성
8.4
소아 사용
8.5
노인 사용
8.6
간 기능 장애
11
설명
12
약리학
12.1
작용 기전
12.2
약력학
12.3
약동학
13
비임상 독성학
13.1
발암성, 돌연변이 유발성, 생식 능력 저해
13.2
동물 독성 및/또는 약리학
14
임상 연구
14.1
이전에 치료받지 않은 ALK 양성 전이성 비소세포폐암
14.2
이전에 치료받은 ALK 양성 전이성 비소세포폐암
16
포장 단위/보관 및 취급
17
환자 상담 정보
- *
- 전문 정보에서 생략된 섹션 또는 하위 섹션은 나열되지 않습니다.
1 적응증 및 용법
ZYKADIA®는 미국 식품의약국(FDA) 승인 시험으로 ALK 양성으로 확인된 종양을 가진 전이성 비소세포폐암(NSCLC) 성인 환자의 치료에 사용됩니다 [투여 및 투약(2.1) 참조].
2 투여 및 관리
2.1
환자 선택
종양 검체에서 ALK 양성이 확인된 전이성 NSCLC 치료를 위해 ZYKADIA를 선택하십시오 [임상 연구(14.1) 참조].
NSCLC에서 ALK 재배열을 검출하기 위한 FDA 승인 검사에 대한 정보는 다음 웹사이트에서 확인할 수 있습니다. http://www.fda.gov/CompanionDiagnostics.
2.2
권장 용량
ZYKADIA의 권장 용량은 질병 진행 또는 허용할 수 없는 독성이 나타날 때까지 음식과 함께 하루에 한 번 450mg을 경구 투여합니다 [임상 약리학(12.3) 참조].
ZYKADIA 복용을 놓친 경우 다음 복용 시간까지 12시간 이내라면 복용량을 보충하십시오.
치료 과정에서 구토가 발생하면 추가 복용량을 투여하지 말고 다음 예정된 ZYKADIA 복용량을 계속 복용하십시오.
2.3
부작용에 대한 용량 조절
| 용량 감소 | 권장 용량 |
| 첫 번째 용량 감소 | 음식과 함께 하루에 한 번 300mg을 경구 투여 |
| 두 번째 용량 감소 | 음식과 함께 하루에 한 번 150mg을 경구 투여 |
식사와 함께 1일 1회 경구 투여 시 150mg을 견딜 수 없는 환자의 경우 ZYKADIA를 중단하십시오.
ZYKADIA의 선택적 유해 반응에 대한 용량 조절은 표 2에 나와 있습니다. 표 2에 나열되지 않은 유해 반응으로 인해 용량 감소가 필요한 경우 ZYKADIA의 일일 용량을 150mg 감소시킵니다.
| 유해 반응 | ZYKADIA 용량 조절 |
| 위장관 유해 반응 [경고 및 주의 사항 (5.1) 참조] | |
| 최적의 항구토제 또는 항설사제 치료에도 불구하고 심각하거나 참을 수 없는 메스꺼움, 구토 또는 설사 | 호전될 때까지 중단한 후 다음 낮은 용량으로 ZYKADIA를 재개합니다. |
| 간 독성 [경고 및 주의 사항 (5.2) 참조] | |
| 총 빌리루빈 수치가 2배 ULN 이하인 경우 ALT 또는 AST 수치가 ULN의 5배를 초과 | 기준선으로 회복되거나 3배 ULN 이하가 될 때까지 중단한 후 다음 낮은 용량으로 ZYKADIA를 재개합니다. |
| 담즙 정체 또는 용혈이 없는 경우 총 빌리루빈 수치가 2배 ULN 초과인 경우 ALT 또는 AST 수치가 ULN의 3배를 초과 | ZYKADIA를 영구적으로 중단합니다. |
| 간질성 폐 질환/폐렴 [경고 및 주의 사항 (5.3) 참조] | |
| 모든 등급의 치료 관련 ILD/폐렴 | ZYKADIA를 영구적으로 중단합니다. |
| QT 간격 연장 [경고 및 주의 사항 (5.4) 참조] | |
| 최소 2개의 별도 ECG에서 QTc 간격이 500msec를 초과 | QTc 간격이 481msec 미만이 될 때까지 또는 기준선 QTc가 481msec 이상인 경우 기준선으로 회복될 때까지 중단한 후 다음 낮은 용량으로 ZYKADIA를 재개합니다. |
| torsades de pointes 또는 다형성 심실 빈맥 또는 심각한 부정맥의 징후/증상과 함께 QTc 간격 연장 | ZYKADIA를 영구적으로 중단합니다. |
| 고혈당증 [경고 및 주의 사항 (5.5) 참조] | |
| 최적의 항고혈당제 치료에도 불구하고 250mg/dL를 초과하는 지속적인 고혈당증 | 고혈당증이 적절히 조절될 때까지 중단한 후 다음 낮은 용량으로 ZYKADIA를 재개합니다. 최적의 의학적 관리로 적절한 고혈당증 조절을 달성할 수 없는 경우 ZYKADIA를 중단합니다. |
| 서맥 [경고 및 주의 사항 (5.6) 참조] | |
| 생명을 위협하지 않는 증상성 서맥 | 증상이 없는 서맥으로 회복되거나 심박수가 60bpm 이상이 될 때까지 중단하고 서맥을 유발하는 것으로 알려진 동반 약물을 평가합니다. 서맥이 다른 약물로 인한 것이 아니면 다음 낮은 용량으로 ZYKADIA를 재개합니다. |
| 개입이 필요한 임상적으로 유의미한 서맥 또는 서맥을 유발하는 것으로 알려진 동반 약물 또는 저혈압을 유발하는 것으로 알려진 약물을 복용하는 환자의 경우 생명을 위협하는 서맥 | 증상이 없는 서맥으로 회복되거나 심박수가 60bpm 이상이 될 때까지 중단합니다. 동반 약물을 조정하거나 중단할 수 있는 경우 빈번한 모니터링과 함께 다음 낮은 용량으로 ZYKADIA를 재개합니다. |
| 서맥을 유발하는 것으로 알려진 동반 약물 또는 저혈압을 유발하는 것으로 알려진 약물을 복용하지 않는 환자의 경우 생명을 위협하는 서맥 | ZYKADIA를 영구적으로 중단합니다. |
| 췌장염 [경고 및 주의 사항 (5.7) 참조] | |
| 리파아제 또는 아밀라아제 수치가 ULN의 2배를 초과 | 1.5배 ULN 미만으로 회복될 때까지 중단한 후 다음 낮은 용량으로 ZYKADIA를 재개합니다. |
| 약어: AST, 아스파르테이트 아미노트랜스퍼라아제; ALT, 알라닌 아미노트랜스퍼라아제; ULN, 정상 상한; ILD, 간질성 폐 질환; ECG, 심전도; bpm, 분당 박동수. | |
2.4
강력한 CYP3A 억제제에 대한 용량 조절
ZYKADIA 치료 중 강력한 CYP3A 억제제와의 병용은 피하십시오 [약물 상호 작용 (7.1), 임상 약리학 (12.3) 참조].
강력한 CYP3A 억제제와의 병용이 불가피한 경우 ZYKADIA 용량을 약 1/3 감소시키고 150mg 용량 단위의 가장 가까운 배수로 반올림합니다. 강력한 CYP3A 억제제 중단 후에는 강력한 CYP3A 억제제를 시작하기 전에 복용했던 ZYKADIA 용량으로 돌아갑니다.
2.5
중증 간 기능 장애 환자에 대한 용량 조절
중증 간 기능 장애 환자(Child-Pugh C)의 경우 ZYKADIA 용량을 약 1/3 감소시키고 150mg 용량 단위의 가장 가까운 배수로 반올림합니다. [특정 인구 집단에서의 사용 (8.6), 임상 약리학 (12.3) 참조].
3 제형 및 함량
캡슐: 불투명한 파란색 캡과 불투명한 흰색 몸체를 가진 150mg 경질 젤라틴 캡슐로, 흰색에서 거의 흰색의 분말을 함유하고 있습니다. 불투명한 파란색 캡은 검은색 잉크로 “LDK 150MG”로 표시되어 있으며, 불투명한 흰색 몸체는 검은색 잉크로 “NVR”로 표시되어 있습니다.
정제: 150mg 필름 코팅 정제, 밝은 파란색, 둥근 모양, 양쪽으로 볼록하며 가장자리가 경사져 있고, 쪼개짐 선이 없으며, 한쪽에는 “NVR”이, 다른 쪽에는 “ZY1”이 각인되어 있습니다.
4 금기사항
없음.
5 경고 및 주의사항
5.1
위장관계 이상반응
공복에 ZYKADIA 750mg을 투여받은 환자에서 중증 위장관계 이상반응이 발생했습니다 [이상반응 (6.1) 참조]. 임상시험에서 ZYKADIA를 투여받은 925명의 환자 중 95%에서 설사, 오심, 구토 또는 복통이 발생했으며, 이 중 중증(3등급 또는 4등급) 사례는 14%였습니다. 설사, 오심, 구토 또는 복통으로 인해 용량 중단 또는 감량이 필요했던 환자는 36%였으며, 치료 중단이 필요했던 환자는 1.6%였습니다.
용량 최적화 연구(ASCEND-8)에서 음식과 함께 ZYKADIA 450mg을 투여받은 환자의 경우 위장관계 이상반응의 발생률과 중증도가 감소했습니다. 음식과 함께 권장 용량인 450mg의 ZYKADIA를 투여받은 108명의 환자 중 79%에서 설사, 오심, 구토 또는 복통이 발생했습니다. 이 중 53%는 1등급 사건이었고 24%는 2등급 사건이었습니다. 한 명의 환자(0.9%)에서 3등급 설사가 발생했고, 한 명의 환자(0.9%)에서 3등급 구토가 발생했습니다. 한 명의 환자(0.9%)는 구토로 인해 용량 조절이 필요했습니다. 11명(10%)의 환자는 적어도 한 번의 용량 중단이 필요한 설사, 오심, 구토 또는 복통을 경험했습니다.
지시에 따라 지사제, 진토제 또는 수액 보충을 포함한 표준 치료법을 사용하여 환자를 모니터링하고 관리하십시오. 위장관계 이상반응이 심각하거나 참을 수 없으며 진토제 또는 지사제에 반응하지 않으면 ZYKADIA 투여를 중단하십시오. 증상이 호전되면 감량된 용량으로 ZYKADIA 투여를 재개하십시오 [용법 및 용량 (2.3) 참조].
5.2
간독성
ZYKADIA를 투여받은 환자에서 약물 유발 간독성이 발생했습니다 [이상반응 (6.1) 참조]. 임상시험에서 925명의 환자 중 28%에서 알라닌 아미노전이효소(ALT)가 정상 상한치(ULN)의 5배를 초과했으며, 16%에서 아스파르테이트 아미노전이효소(AST)가 ULN의 5배를 초과했습니다. 임상시험에서 ALT가 ULN의 3배를 초과하고 총 빌리루빈이 ULN의 2배를 초과하는 동시 상승이 알칼리성 인산분해효소가 ULN의 2배 미만인 경우는 0.3%의 환자에서 발생했습니다. 간독성으로 인해 약 1%의 환자가 영구적으로 치료를 중단해야 했습니다.
ALT, AST, 총 빌리루빈을 포함한 간 기능 검사를 통해 매달 한 번씩, 그리고 임상적으로 필요에 따라 모니터링하고, 트랜스아미나제 상승이 나타나는 환자의 경우 더 자주 검사하십시오. 이상반응의 중증도에 따라 ZYKADIA 투여를 중단하고 감량된 용량으로 재개하거나 ZYKADIA 투여를 영구적으로 중단하십시오 [용법 및 용량 (2.3) 참조].
5.3
간질성 폐질환/폐렴
ZYKADIA를 투여받은 환자에서 중증, 생명을 위협하거나 치명적인 간질성 폐질환(ILD)/폐렴이 발생했습니다 [이상반응 (6.1) 참조]. 임상시험에서 ZYKADIA를 투여받은 925명의 환자 중 2.4%에서 ILD/폐렴이 보고되었습니다. 3등급 또는 4등급 ILD/폐렴은 1.3%의 환자에서 보고되었으며, 치명적인 사건은 0.2%의 환자에서 보고되었습니다. ILD/폐렴으로 인해 임상시험에서 ZYKADIA를 중단한 환자는 10명(1.1%)이었습니다.
ILD/폐렴을 나타내는 폐 증상이 있는지 환자를 모니터링하십시오. ILD/폐렴의 다른 잠재적 원인을 배제하고 치료 관련 ILD/폐렴으로 진단된 환자의 경우 ZYKADIA 투여를 영구적으로 중단하십시오 [용법 및 용량 (2.3) 참조].
5.4
QT 간격 연장
ZYKADIA를 투여받은 환자에서 심실 빈맥(예: 다형성 심실 빈맥) 또는 갑작스러운 사망 위험을 증가시킬 수 있는 QTc 간격 연장이 발생했습니다 [이상반응 (6.1) 참조]. 임상시험에서 기준치 이후 심전도(ECG) 평가를 한 번 이상 받은 919명의 환자 중 6%에서 QTc가 기준치보다 60msec 이상 증가했습니다. 공복에 ZYKADIA 750mg을 복용한 환자의 약 1.3%에서 QTc가 500msec를 초과하는 것으로 나타났습니다. ZYKADIA는 농도 의존적으로 QTc 간격을 증가시킵니다 [임상 약리학 (12.2) 참조]. 임상시험에서 QTc 연장으로 인해 ZYKADIA를 중단한 환자는 0.2%였습니다.
가능하면 선 Romano-Ward 증후군 환자에게 ZYKADIA를 사용하지 마십시오. 울혈성 심부전, 서맥, 전해질 이상이 있거나 QTc 간격을 연장하는 것으로 알려진 약물을 복용하는 환자의 경우 ECG 및 전해질을 주기적으로 모니터링하십시오. 이상반응의 중증도에 따라 ZYKADIA 투여를 중단하고 감량된 용량으로 재개하거나 ZYKADIA 투여를 영구적으로 중단하십시오 [용법 및 용량 (2.3) 참조].
5.5
고혈당증
ZYKADIA를 투여받은 환자에서 고혈당증이 발생했습니다 [이상반응 (6.1) 참조]. 임상시험에서 925명의 환자 중 13%에서 실험실적 수치를 기준으로 3등급 또는 4등급 고혈당증이 발생했습니다.
ZYKADIA 치료를 시작하기 전에 공복 혈청 포도당을 모니터링하고 이후 임상적으로 필요에 따라 주기적으로 모니터링하십시오. 지시에 따라 혈당강하제를 시작하거나 최적화하십시오. 이상반응의 중증도에 따라 ZYKADIA 투여를 중단하고 감량된 용량으로 재개하거나 ZYKADIA 투여를 영구적으로 중단하십시오 [용법 및 용량 (2.3) 참조].
5.6
서맥
ZYKADIA로 치료받은 환자에서 서맥이 발생했습니다 [부작용 (6.1) 참조]. 임상 연구에서 분당 50회 미만의 심박수로 정의되는 동성 서맥이 925명의 환자 중 1.1%에서 새로운 소견으로 나타났습니다. 서맥은 환자의 1%에서 부작용으로 보고되었습니다. 서맥으로 인해 치료를 중단한 환자는 없었으며 0.1%는 치료를 일시 중단한 후 용량을 줄여 다시 투여했습니다.
가능한 한 서맥을 유발하는 것으로 알려진 다른 제품(예: 베타 차단제, 비디하이드로피리딘 칼슘 채널 차단제, 클로니딘 및 디곡신)과 ZYKADIA를 병용하지 마십시오. 심박수와 혈압을 정기적으로 모니터링하십시오. 부작용의 심각도에 따라 서맥이 해결되면 ZYKADIA를 보류하고 용량을 줄여 재투여하거나 ZYKADIA를 영구적으로 중단하십시오 [용량 및 투여(2.3) 참조].
5.7
췌장염
ZYKADIA로 치료받은 환자에서 췌장염이 발생했습니다 [부작용 (6.1) 참조]. 임상 연구에서 ZYKADIA를 투여받은 환자의 1% 미만에서 사망 1건을 포함하여 췌장염이 발생했습니다. 임상 연구에서 ZYKADIA를 투여받은 환자의 7%에서 3등급 또는 4등급 아밀라아제 수치 상승이 나타났고, 14%에서 3등급 또는 4등급 리파아제 수치 상승이 나타났습니다.
ZYKADIA 치료를 시작하기 전과 이후에 임상적으로 필요에 따라 리파아제와 아밀라아제를 모니터링하십시오. 실험실 검사 이상의 심각도에 따라 ZYKADIA를 보류하고 용량을 줄여 재투여하십시오 [용량 및 투여(2.3) 참조].
5.8
배아-태아 독성
ZYKADIA는 작용 기전 및 동물 연구 결과에 따라 임산부에게 투여 시 태아에게 해를 끼칠 수 있습니다. 동물 연구에서 임신 기간 중 권장 사람 용량 미만의 모체 혈장 노출에서 쥐와 토끼에게 ceritinib을 투여한 결과 쥐와 토끼에서 골격 기형이 증가했습니다.
임산부에게 태아에 대한 잠재적 위험을 알리십시오. 가임 여성에게는 ZYKADIA 치료 중 및 치료 종료 후 6개월 동안 효과적인 피 contraception을 사용하도록 권고하십시오. 유전 독성 가능성에 따라 가임 여성 파트너가 있는 남성에게는 ZYKADIA 치료 중 및 치료 종료 후 3개월 동안 콘돔을 사용하도록 권고하십시오 [특정 집단에서의 사용(8.1, 8.3), 비임상 독성학(13.1) 참조].
6 부작용
다음 임상적으로 유의미한 유해 반응은 라벨링의 다른 부분에서 설명되어 있습니다.
- 위장관 유해 반응 [경고 및 주의 사항 (5.1) 참조]
- 간 독성 [경고 및 주의 사항 (5.2) 참조]
- 간질성 폐 질환/폐렴 [경고 및 주의 사항 (5.3) 참조]
- QT 간격 연장 [경고 및 주의 사항 (5.4) 참조]
- 고혈당증 [경고 및 주의 사항 (5.5) 참조]
- 서맥 [경고 및 주의 사항 (5.6) 참조]
- 췌장염 [경고 및 주의 사항 (5.7) 참조]
6.1
임상 시험 경험
임상 시험은 다양한 조건에서 수행되므로, 약물의 임상 시험에서 관찰된 유해 반응 발생률은 다른 약물의 임상 시험에서 관찰된 발생률과 직접 비교할 수 없으며, 실제로 관찰된 발생률을 반영하지 않을 수 있습니다.
경고 및 주의 사항 섹션의 데이터는 아래에 설명된 ASCEND-4 및 ASCEND-1을 포함한 7개의 임상 연구에서 ALK 양성 NSCLC 환자 925명을 대상으로 공복 상태에서 ZYKADIA 750mg을 1일 1회 투여한 결과를 반영합니다. 이는 무작위 배정된 활성 대조군 연구, 단일군 연구 2건, 용량 증량 연구 2건을 포함합니다. 이 연구에 등록된 환자 대부분은 NSCLC에 대한 화학 요법 및/또는 크리조티닙으로 사전 치료를 받았습니다. 이 925명의 환자 중 가장 흔한 유해 반응(발생률 ≥ 25%)은 설사, 메스꺼움, 구토, 피로, 복통, 식욕 감소 및 체중 감소였습니다. 공복 상태에서 ZYKADIA 750mg으로 치료를 시작한 환자의 약 45%는 최소한 1회 이상 용량 감소가 필요한 유해 반응을 보였고, 환자의 66%는 최소한 1회 이상 용량 중단이 필요한 유해 반응을 보였습니다. 모든 원인으로 인한 최초 용량 감소까지의 중앙값은 7주였습니다.
용량 최적화 연구: 음식과 함께 1일 450mg 투여 요법
ASCEND-8은 용량 최적화 연구로, 음식과 함께 ZYKADIA 450mg을 1일 1회 투여한 그룹(N = 108)과 공복 상태에서 750mg을 1일 1회 투여한 그룹(N = 110)을 비교했습니다. 이 연구는 사전 치료를 받은 환자와 치료를 받지 않은 환자 모두를 대상으로 ALK 양성 NSCLC 환자를 대상으로 진행되었습니다. 음식과 함께 ZYKADIA 450mg을 투여한 그룹의 전반적인 안전성 프로파일은 ZYKADIA 750mg을 공복 상태로 투여한 그룹과 일치했지만, 위장관 유해 반응은 감소했으며, 비슷한 정상 상태 노출을 달성했습니다. [임상 약리학 (12.3) 참조]. 음식과 함께 450mg을 투여한 그룹에서 가장 흔한 유해 반응(발생률 ≥ 25%)은 설사, 메스꺼움, 복통, 구토 및 피로였습니다. 음식과 함께 ZYKADIA 450mg을 투여한 환자의 경우 위장관 유해 반응(설사 59%, 메스꺼움 43%, 구토 38%)의 발생률과 심각도가 감소했습니다. 3등급 이상의 유해 반응은 2명의 환자(1.9%)에게서 보고되었습니다. 1명의 환자에게서 3등급 설사와 1명의 환자에게서 3등급 구토가 보고되었습니다. [경고 및 주의 사항 (5.1) 참조].
음식과 함께 ZYKADIA 450mg을 투여한 환자의 경우, 24%의 환자가 최소한 1회 이상 용량 감소가 필요한 유해 반응을 보였고, 56%의 환자가 최소한 1회 이상 용량 중단이 필요한 유해 반응을 보였습니다. 모든 원인으로 인한 최초 용량 감소까지의 중앙값은 8주였습니다.
사전 치료를 받지 않은 ALK 양성 전이성 NSCLC
ZYKADIA의 안전성은 ASCEND-4에서 평가되었습니다. ASCEND-4는 사전 치료를 받지 않은 ALK 양성 NSCLC 환자 376명을 대상으로 진행된 개방형, 무작위 배정, 활성 대조군 다기관 연구입니다. [임상 연구 (14.1) 참조]. 환자는 공복 상태에서 ZYKADIA 750mg을 1일 1회 투여받았습니다(N = 189) 또는 화학 요법과 유지 화학 요법을 받았습니다(N = 187). 화학 요법 요법은 페메트렉세드(500mg/m2)와 시스플라틴(75mg/m2) 또는 카보플라틴[곡선 아래 면적(AUC) 5-6mg*min/mL]을 연구자의 선택에 따라 21일마다 투여했습니다. 진행성 질환 없이 4주기의 화학 요법을 완료한 환자는 21일마다 단독 요법으로 페메트렉세드(500mg/m2)를 유지 요법으로 투여받았습니다. ZYKADIA에 대한 노출의 중앙값은 18개월이었습니다.
연구 대상 인구의 인구 통계적 특징은 여성 57%, 중앙값 연령 54세(범위 22-81세), 65세 이상 22%, 백인 54%, 아시아인 42%, 흑인 2%, 기타 인종 2%였습니다. 환자는 유럽(53%), 아시아 태평양(42%), 남미(5%) 지역에 등록되었습니다. 환자 대부분은 선암(97%)이었고, 담배를 피운 적이 없었습니다(61%). 32%의 환자는 선별 검사 시 뇌 전이가 있었습니다.
ZYKADIA로 치료받은 환자 4명에게서 다음과 같은 치명적인 유해 반응이 발생했습니다. 심근 경색, 호흡기 감염, 폐렴 및 원인 불명.
ZYKADIA로 치료받은 환자의 38%에게서 심각한 유해 반응이 보고되었습니다. 가장 흔한 심각한 유해 반응은 폐렴(4%), 흉막 삼출(4%), 구토(4%), 메스꺼움(3%), 호흡 곤란(3%), 고혈당증(3%), AST 증가(2%), 폐 감염(2%), 심낭 삼출(2%)이었습니다.
ZYKADIA로 치료받은 환자 중 유해 반응으로 인해 용량 중단이 발생한 환자는 77%, 용량 감소가 필요했던 환자는 66%, 치료 중단으로 이어진 유해 반응을 보인 환자는 12%였습니다. ZYKADIA로 치료받은 환자의 10% 이상에서 보고된 가장 흔한 유해 반응(용량 중단 또는 감소로 이어짐)은 다음과 같습니다. ALT 증가(48%), AST 증가(34%), 구토(15%), 혈중 크레아티닌 증가(14%), 감마-글루타밀 트랜스펩티다제(GGT) 증가(13%), 설사(13%), 메스꺼움(13%). ASCEND-4에서 환자의 1% 이상에서 ZYKADIA 중단으로 이어진 가장 흔한 유해 반응은 혈중 크레아티닌 증가(2.1%), 아밀라아제 증가(1.1%), 리파아제 증가(1.1%)였습니다.
표 3과 4는 ASCEND-4에서 유해 반응과 실험실 검사 이상을 각각 요약한 것입니다.
| ZYKADIA N = 189 |
화학 요법 N = 175a |
|||
| 모든 등급 | 3-4등급 | 모든 등급 | 3-4등급 | |
| % | % | % | % | |
| 위장** | ||||
| 설사 | 85 | 4.8 | 11 | 1.1 |
| 메스꺼움 | 69 | 2.6 | 55 | 5 |
| 구토 | 67 | 5 | 36 | 6 |
| 복통b | 40 | 3.7 | 13 | 0 |
| 변비 | 20 | 0 | 22 | 0 |
| 식도 장애c | 15 | 0.5 | 8 | 0.6 |
| 일반 | ||||
| 피로d | 45 | 7 | 49 | 6 |
| 비심장성 흉통 | 21 | 1.1 | 10 | 0.6 |
| 요통 | 19 | 1.6 | 18 | 2.3 |
| 발열 | 19 | 0 | 14 | 1.1 |
| 사지 통증 | 13 | 0 | 7 | 0 |
| 근골격계 통증 | 11 | 0.5 | 6 | 0.6 |
| 가려움증 | 11 | 0.5 | 5 | 0 |
| 대사 및 영양 | ||||
| 식욕 감소 | 34 | 1.1 | 32 | 1.1 |
| 체중 감소 | 24 | 3.7 | 15 | 0.6 |
| 호흡기 | ||||
| 기침 | 25 | 0 | 17 | 0 |
| 피부 | ||||
| 발진e | 21 | 1.1 | 8 | 0.6 |
| 신경계 | ||||
| 두통 | 19 | 0.5 | 13 | 1.1 |
| 현기증 | 12 | 1.1 | 10 | 0.6 |
| 심장 | ||||
| QT 연장 | 12 | 2.6 | 1.1 | 0.6 |
| 심낭염f | 4.2 | 1.6 | 2.3 | 1.1 |
| *국립암연구소의 부작용에 대한 일반 용어 기준 (버전 4.03). **음식과 함께 권장 용량 450mg으로 투여 시 위장관 부작용 빈도에 대한 정보는 [경고 및 주의 사항 (5.1), 부작용 (6.1) 참조]. a화학 요법에 무작위 배정된 12명의 환자는 연구 약물을 투여받지 않았습니다. b복통 (복통, 상복부 통증, 복부 불편감, 상복부 불편감). c식도 장애 (소화 불량, 위식도 역류 질환, 연하 곤란). d피로 (피로 및 무력증). e발진 (발진, 여드름 모양 피부염, 구진-반점 발진). f심낭염 (심낭 삼출 및 심낭염). |
||||
ZYKADIA 750mg를 공복 상태에서 투여받은 환자의 2% 이상에서 발생한 추가적인 임상적으로 유의미한 이상 반응은 다음과 같습니다: 시력 장애(시력 저하, 시력 흐림, 광시증, 조절 장애, 노안, 시력 감소 또는 유리체 부유물을 포함한 4%), 서맥(4%), ILD/폐렴(2%), 간 독성(2%) 및 신부전(2%). 또한, 광과민성 반응은 환자의 1.1%에서 보고되었습니다.
| ZYKADIA N = 189 |
화학 요법 N = 175a |
|||
| 모든 등급 | 3-4등급 | 모든 등급 | 3-4등급 | |
| % | % | % | % | |
| 화학 | ||||
| ALT 증가 | 91 | 34 | 65 | 3.4 |
| AST 증가 | 86 | 21 | 58 | 2.3 |
| GGT 증가 | 84 | 49 | 67 | 10 |
| 알칼리성 포스파타제 증가 | 81 | 12 | 47 | 1.7 |
| 크레아티닌 증가 | 77 | 4.2 | 37 | 0.6 |
| 고혈당증 | 53 | 10 | 67 | 10 |
| 저인산혈증 | 38 | 3.7 | 27 | 4.0 |
| 아밀라아제 증가 | 37 | 8 | 43 | 4.5 |
| 고빌리루빈혈증(총) | 15 | 0.5 | 6 | 0.6 |
| 리파아제 증가b | 13 | 6 | 7 | 0.6 |
| 혈액학 | ||||
| 빈혈 | 67 | 4.2 | 84 | 11 |
| 호중구 감소증 | 27 | 2.1 | 58 | 20 |
| 혈소판 감소증 | 16 | 1.0 | 38 | 4.6 |
| 약어: ALT, 알라닌 아미노 전이효소; AST, 아스파르트산 아미노 전이효소; GGT, 감마-글루타밀 트랜스펩티다아제. *국립 암 연구소의 이상 반응 공통 용어 기준(버전 4.03). a화학 요법에 무작위 배정된 12명의 환자는 연구 약물을 투여받지 않았습니다. bZYKADIA군에서는 기준 리파아제 실험실 검사를 받은 환자가 없었고, 기준 이후 검사를 받은 환자는 112명이었습니다. 화학 요법군에서는 기준 리파아제 실험실 검사를 받은 환자가 1명이었지만 기준 이후 검사를 받은 환자는 없었고, 기준 이후 검사를 받은 환자는 49명이었습니다. |
||||
ALK 양성 전이성 비소세포폐암 치료 이력이 있는 환자
ZYKADIA의 안전성은 ASCEND-1에서 평가되었으며, ASCEND-1은 255명의 ALK 양성 환자(ZYKADIA를 공복 상태에서 1일 750mg 용량으로 투여받은 246명의 NSCLC 환자와 9명의 다른 암 환자)를 대상으로 한 다기관, 단일군, 공개 표지 임상 연구입니다. [임상 연구(14.2) 참조]. ZYKADIA에 대한 노출의 중앙값 기간은 6개월이었습니다.
연구 대상군의 특징은 다음과 같습니다. 중앙값 연령 53세, 65세 미만(84%), 여성(53%), 백인(63%), 아시아인(34%), NSCLC 선암 조직학(90%), 비흡연자 또는 과거 흡연자(97%), 동부 협력 종양학 그룹 수행 상태(ECOG PS) 0 또는 1(89%), 뇌 전이(49%), 이전 치료 횟수 2회 이상(67%).
ZYKADIA로 치료받은 환자에서 치명적인 유해 반응은 환자의 5%에서 발생했으며, 다음과 같습니다. 폐렴(4명), 호흡 부전, ILD/폐렴, 기흉, 위 출혈, 일반적인 신체 건강 악화, 폐 결핵, 심장 탐폰, 패혈증(각 1명).
ASCEND-1에서 환자의 2% 이상에서 보고된 심각한 유해 반응은 경련, 폐렴, ILD/폐렴, 호흡 곤란, 탈수, 고혈당 및 메스꺼움이었습니다.
유해 반응으로 인한 용량 감소는 ZYKADIA로 치료받은 환자의 59%에서 발생했습니다. ZYKADIA로 치료받은 환자의 10% 이상에서 보고된 용량 감소 또는 중단으로 이어진 가장 흔한 유해 반응은 다음과 같습니다. ALT 증가(29%), 메스꺼움(20%), AST 증가(16%), 설사(16%), 구토(16%). 유해 반응으로 인한 치료 중단은 ZYKADIA로 치료받은 환자의 10%에서 발생했습니다. ASCEND-1에서 환자의 1% 이상에서 중단으로 이어진 가장 흔한 유해 반응은 폐렴, ILD/폐렴 및 식욕 감소였습니다.
표 5와 6은 각각 ASCEND-1에서 유해 반응과 실험실 이상을 요약한 것입니다.
| ZYKADIA N = 255 |
||
| 모든 등급 | 등급 3-4 | |
| % | % | |
| 위장** | ||
|
설사 |
86 | 6 |
|
메스꺼움 |
80 | 4 |
|
구토 |
60 | 4 |
|
복통a |
54 | 2 |
|
변비 |
29 | 0 |
|
식도 장애b |
16 | 1 |
| 일반 | ||
|
피로c |
52 | 5 |
| 대사 및 영양 | ||
|
식욕 감소 |
34 | 1 |
| 피부 | ||
|
발진d |
16 | 0 |
| 호흡기 | ||
|
간질성 폐 질환/폐렴 |
4 | 3 |
| 약어: ALK, 역형성 림프종 키나아제. *국립 암 연구소 유해 사건에 대한 일반 용어 기준(버전 4.03). **음식과 함께 권장 용량 450mg의 위장계 유해 반응 빈도에 대해 [경고 및 주의 사항(5.1), 유해 반응(6.1) 참조]. a복통(복통, 상복부 통증, 복부 불편함 및 상복부 불편함). b식도 장애(소화 불량, 위식도 역류 질환 및 연하 곤란). c피로(피로 및 무력증). d발진(발진, 구진성 발진 및 여드름 모양 피부염). |
||
ZYKADIA 750 mg를 공복 상태에서 투여받은 환자의 2% 이상에서 발생한 추가적인 임상적으로 유의미한 이상 반응은 신경병증(17%, 감각 이상, 근력 저하, 보행 장애, 말초 신경병증, 감각 저하, 말초 감각 신경병증, 이상 감각, 신경통, 말초 운동 신경병증, 저긴장증 또는 다발성 신경병증 포함), 시력 장애(9%, 시력 저하, 시력 흐림, 광시증, 조절 장애, 노안 또는 시력 감소 포함), QT 연장(4%) 및 서맥(3%)이었습니다. 또한, 광과민성 이상 반응이 환자의 1.2%에서 보고되었습니다.
| ZYKADIA N = 255 |
||
| 모든 등급 | 3-4등급 | |
| % | % | |
| 혈액학 | ||
|
빈혈 |
84 | 5 |
| 화학 | ||
|
ALT 증가 |
80 | 27 |
|
AST 증가 |
75 | 13 |
|
크레아티닌 증가 |
58 | 2 |
|
고혈당증 |
49 | 13 |
|
저인산혈증 |
36 | 7 |
|
리파아제 증가 |
28 | 10 |
|
고빌리루빈혈증(총) |
15 | 1 |
| 약어: ALT, 알라닌 아미노트랜스퍼라제; AST, 아스파르테이트 아미노트랜스퍼라제; ALK, 역형성 림프종 키나아제. *국립 암 연구소의 이상 반응에 대한 일반 용어 기준(버전 4.03). |
||
7 약물 상호작용
7.1
Effect of Other Drugs on ZYKADIA
Strong CYP3A Inhibitors
강력한 CYP3A4/P-gp 억제제(케토코나졸)는 세리티닙의 전신 노출을 증가시켰습니다 [임상 약리학 (12.3) 참조]. 이는 ZYKADIA의 부작용 발생률과 심각도를 증가시킬 수 있습니다. ZYKADIA 치료 중 강력한 CYP3A 억제제와의 병용 사용은 피하십시오. 강력한 CYP3A 억제제와의 병용 사용이 불가피한 경우 ZYKADIA 용량을 줄이십시오 [용법 및 용량 (2.4) 참조].
자몽과 자몽 주스는 CYP3A를 억제할 수 있으므로 섭취하지 마십시오.
Strong CYP3A Inducers
강력한 CYP3A4/P-gp 유도제(리팜핀)는 세리티닙의 전신 노출을 감소시켰습니다 [임상 약리학 (12.3) 참조]. 이는 ZYKADIA의 효능을 감소시킬 수 있습니다. ZYKADIA 치료 중 강력한 CYP3A 유도제와의 병용 사용은 피하십시오.
7.2
Effect of ZYKADIA on Other Drugs
CYP3A Substrates
세리티닙은 민감한 CYP3A 기질(미다졸람)의 전신 노출을 증가시켰습니다 [임상 약리학 (12.3) 참조]. ZYKADIA와 민감한 CYP3A 기질의 병용 투여는 피하십시오. 병용 투여가 불가피한 경우 민감한 CYP3A 기질(들)의 용량 감소를 고려하십시오. ZYKADIA를 다른 CYP3A 기질과 병용 투여하는 경우 강력한 CYP3A 억제제와의 용량 권장 사항에 대한 CYP3A 기질 라벨을 참조하십시오.
CYP2C9 Substrates
세리티닙은 CYP2C9 기질(와파린)의 전신 노출을 증가시켰습니다 [임상 약리학 (12.3) 참조]. 와파린과의 병용 투여가 불가피한 경우 와파린의 항응고 효과가 증가할 수 있으므로 INR 모니터링 빈도를 높이십시오.
최소한의 농도 변화가 심각한 독성으로 이어질 수 있는 CYP2C9 기질과 ZYKADIA의 병용 투여는 피하십시오. 이러한 CYP2C9 기질과의 병용 투여가 불가피한 경우 병용 투여된 CYP2C9 기질의 용량 감소를 고려하십시오.
7.3
Drugs That Prolong QT Interval
ZYKADIA는 농도 의존적으로 QTc 간격을 연장시킵니다. 가능한 경우 ZYKADIA를 QTc 간격을 연장시킬 가능성이 있는 것으로 알려진 다른 제품과 병용 투여하지 마십시오 [경고 및 주의 사항 (5.4), 임상 약리학 (12.2) 참조].
7.4
Drugs That Cause Bradycardia
ZYKADIA는 서맥을 유발할 수 있습니다. 가능한 경우 ZYKADIA를 서맥을 유발하는 것으로 알려진 다른 제품과 병용 투여하지 마십시오 [경고 및 주의 사항 (5.6), 임상 약리학 (12.2) 참조].
8 특정 집단에서의 사용
8.1
임신
위험 요약
동물 연구 및 작용 기전 [임상 약리학 (12.1) 참조]을 기반으로 ZYKADIA는 임산부에게 투여하면 태아에게 해를 끼칠 수 있습니다. 임산부에 대한 ZYKADIA 사용에 대한 제한된 이용 가능한 데이터는 위험을 알리기에 충분하지 않습니다. 임신 중 기관 형성 기간 동안 임신 랫트와 토끼에게 ceritinib를 투여한 결과, 권장 인간 용량보다 낮은 모체 혈장 노출에서 랫트와 토끼의 골격 이상이 증가했습니다. [데이터 참조] 임산부에게 태아에 대한 잠재적 위험을 알립니다.
미국 일반 인구에서 임상적으로 인식되는 임신에서 주요 선천적 기형 및 유산의 추정 배경 위험은 각각 2%에서 4% 및 15%에서 20%입니다.
데이터
동물 데이터
임신 랫트에게 기관 형성 기간 동안 매일 ceritinib를 투여한 배아-태아 발달 연구에서, 권장 용량에서 AUC에 의한 인간 노출의 0.5배 미만인 50mg/kg만큼 낮은 용량에서 용량 의존적 골격 이상이 관찰되었습니다. 발견에는 지연된 골화 및 골격 변이가 포함되었습니다.
기관 형성 기간 동안 매일 ceritinib를 투여한 임신 토끼에서, 권장 용량에서 AUC에 의한 인간 노출의 약 0.015배인 2mg/kg/일 이상의 용량에서 불완전한 골화를 포함한 용량 의존적 골격 이상이 관찰되었습니다. 권장 용량에서 AUC에 의한 인간 노출의 약 0.13배인 10mg/kg/일 이상의 용량에서 결손 또는 위치가 잘못된 담낭 및 식도 뒤 쇄골하 심장 동맥을 포함한 내장 기형이 낮은 빈도로 관찰되었습니다. 35mg/kg 이상의 용량에서 토끼에서 모체 독성 및 유산이 발생했습니다. 또한 50mg/kg의 용량에서 토끼에서 배아 사망이 관찰되었습니다.
8.2
수유
위험 요약
모유에서 ceritinib 또는 그 대사산물의 존재, ceritinib가 모유 수유 아동에게 미치는 영향 또는 모유 생산에 미치는 영향에 대한 데이터는 없습니다. 모유 수유 아동에게 심각한 부작용이 발생할 가능성이 있으므로, 여성에게 ZYKADIA 치료 중 및 치료 종료 후 2주 동안 모유 수유를 하지 않도록 조언합니다.
8.3
생식 능력이 있는 여성 및 남성
임신 검사
ZYKADIA를 시작하기 전에 생식 능력이 있는 여성의 임신 상태를 확인합니다. [특정 인구에 대한 사용 (8.1) 참조].
피임
ZYKADIA는 임산부에게 투여하면 태아에게 해를 끼칠 수 있습니다. [특정 인구에 대한 사용 (8.1) 참조].
여성
생식 능력이 있는 여성에게 ZYKADIA 치료 중 및 치료 종료 후 6개월 동안 효과적인 피임법을 사용하도록 조언합니다.
남성
유전 독성 가능성을 고려하여 생식 능력이 있는 여성 파트너가 있는 남성에게 ZYKADIA 치료 중 및 치료 종료 후 3개월 동안 콘돔을 사용하도록 조언합니다. [비임상 독성학 (13.1) 참조].
8.5
노인 사용
ZYKADIA의 임상 연구에 참여한 925명의 환자 중 18%가 65세 이상이었고, 5%가 75세 이상이었습니다. 이러한 대상과 젊은 대상 간에 안전성 또는 유효성에 대한 전반적인 차이가 관찰되지 않았습니다.
8.6
간 기능 장애
중증 간 기능 장애(Child-Pugh C) 환자의 경우 ZYKADIA 용량을 줄입니다. [용량 및 투여 (2.5) 참조] 경증(Child-Pugh A) 또는 중등도(Child-Pugh B) 간 기능 장애 환자의 경우 용량 조절은 권장되지 않습니다.
11 설명
세리티닙은 경구 투여용 키나아제 억제제입니다. 세리티닙의 분자식은 C28H36N5O3ClS입니다. 분자량은 558.14 g/mol입니다. 세리티닙은 화학적으로 5-클로로-N4-[2-[(1-메틸에틸)설포닐]페닐]-N2-[5-메틸-2-(1-메틸에톡시)-4-(4-피페리디닐)페닐]-2,4-피리미딘디아민으로 설명됩니다.
세리티닙의 화학 구조는 아래와 같습니다.
세리티닙은 백색에서 거의 백색 또는 연한 노란색 분말입니다.
ZYKADIA는 150mg의 세리티닙을 함유한 인쇄된 경질 젤라틴 캡슐로 제공되며, 다음과 같은 비활성 성분이 포함되어 있습니다: 콜로이드성 실리카, 경질 젤라틴 캡슐 껍질, 저치환 히드록시프로필 셀룰로오스, 마그네슘 스테아레이트, 미결정 셀룰로오스 및 나트륨 전분 글리콜레이트. 캡슐 껍질은 FD&C 블루 # 2, 젤라틴 및 이산화티탄으로 구성됩니다.
ZYKADIA는 150mg의 세리티닙을 함유한 필름 코팅 정제로 제공되며, 다음과 같은 비활성 성분이 포함되어 있습니다: 콜로이드성 실리카, 크로스카멜로오스 나트륨, 저치환 히드록시프로필 셀룰로오스, 마그네슘 스테아레이트, 미결정 셀룰로오스 및 포비돈. 정제 코팅에는 FD&C 블루 # 2 알루미늄 레이크, 히프로멜로오스, 폴리에틸렌 글리콜 4000, 활석 및 이산화티탄이 포함되어 있습니다.
12 임상약리학
12.1
작용 기전
세리티닙은 키나아제 억제제입니다. 세리티닙 억제의 표적은 임상적으로 관련된 농도에서 생화학적 또는 세포 분석에서 확인된 ALK, 인슐린 유사 성장 인자 1 수용체 (IGF-1R), 인슐린 수용체 (InsR) 및 ROS1을 포함합니다. 이 중 세리티닙은 ALK에 대해 가장 활성이 높습니다. 세리티닙은 ALK의 자가 인산화, 하류 신호 전달 단백질 STAT3의 ALK 매개 인산화 및 in vitro 및 in vivo 분석에서 ALK 의존성 암 세포의 증식을 억제했습니다.
세리티닙은 EML4-ALK 및 NPM-ALK 융합 단백질을 발현하는 세포주에서 in vitro 증식을 억제했으며 마우스와 랫트에서 EML4-ALK 양성 NSCLC 이종 이식 성장을 용량 의존적으로 억제했습니다. 세리티닙은 임상적으로 관련 범위 내의 농도에서 크리조티닙에 대한 내성이 입증된 EML4-ALK 양성 NSCLC 이종 이식을 가진 마우스에서 용량 의존적인 항 종양 활성을 나타냈습니다.
12.2
약력학
심장 전기 생리학
금식 상태에서 ZYKADIA 750mg을 1일 1회 투여받은 919명의 환자 중 12명(1.3%)은 기준선 ECG 평가 후 적어도 한 번 이상 QTc > 500msec를 보였고 58명(6%)은 기준선 QTc > 60msec 증가를 보였습니다. ASCEND-4에서 평균 정상 상태 농도에서 QTc 데이터의 중심 경향 분석 결과, 금식 상태에서 ZYKADIA 750mg을 1일 1회 투여했을 때 QTc의 양측 90% CI 상한은 15.3msec였습니다. 약동학/약력학 분석 결과 농도 의존적인 QTc 간격 연장이 시사되었습니다 [경고 및 주의 사항 (5.4) 참조].
925명의 환자 중 10명(1.1%)은 분당 50회 미만으로 정의된 서맥을 보였습니다 [경고 및 주의 사항 (5.6) 참조].
12.3
약동학
환자에게 ZYKADIA를 단회 경구 투여한 후, 금식 상태에서 50mg에서 750mg까지 용량에 비례하여 AUC 및 Cmax가 증가했습니다.
금식 상태에서 ZYKADIA 750mg을 1일 1회 투여한 후, 15일 만에 정상 상태에 도달했으며 3주 후 기하 평균 누적 비율은 6.2였습니다. 금식 상태에서 1일 1회 50mg에서 750mg까지 반복 투여 후, 용량에 비례하여 더 높은 수준으로 전신 노출이 증가했습니다.
흡수
환자에게 ZYKADIA를 단회 경구 투여한 후, 세리티닙의 혈장 최고 농도(Cmax)는 약 4~6시간에 도달했습니다.
식품 효과
건강한 피험자에게 ZYKADIA 캡슐 500mg을 단회 투여한 식품 효과 연구 결과, 고지방 식사(약 1000칼로리 및 58g 지방 함유)는 세리티닙 AUC를 73% 증가시키고 Cmax를 41% 증가시켰으며 저지방 식사(약 330칼로리 및 9g 지방 함유)는 세리티닙 AUC를 58% 증가시키고 Cmax를 43% 증가시켰습니다. 금식 상태와 비교했습니다.
건강한 피험자에게 ZYKADIA 정제 750mg을 단회 투여한 식품 효과 연구 결과, 고지방 식사(약 1000칼로리 및 58g 지방 함유)는 세리티닙 AUC를 64% 증가시키고 Cmax를 58% 증가시켰으며 저지방 식사(약 330칼로리 및 9g 지방 함유)는 세리티닙 AUC를 39% 증가시키고 Cmax를 42% 증가시켰습니다. 금식 상태와 비교했습니다.
용량 최적화 연구: 식사와 함께 1일 450mg 투여 요법
식사와 함께 ZYKADIA 캡슐을 1일 450mg(약 100~500칼로리 및 1.5~15g 지방 함유) 또는 금식 상태에서 1일 750mg을 투여받은 환자를 대상으로 한 용량 최적화 연구(ASCEND-8)에서, 식사와 함께 450mg 투여군과 금식 상태에서 750mg 투여군 간에 세리티닙의 전신 정상 상태 노출(AUC)에 임상적으로 의미 있는 차이가 없었습니다.
분포
세리티닙은 약물 농도와 무관하게 인간 혈장 단백질에 97% 결합합니다. 환자에게 금식 상태에서 ZYKADIA 750mg을 단회 투여한 후, 기하 평균 명백 분포 용적(Vd/F)은 4230L입니다. 세리티닙은 혈장에 비해 적혈구에 약간 더 선호도를 보이며, in vitro 혈액-혈장 비율의 평균은 1.35입니다.
배설
환자에게 금식 상태에서 ZYKADIA 750mg을 단회 투여한 후, 세리티닙의 기하 평균 명백 혈장 말기 반감기(t1/2)는 41시간이었습니다. 세리티닙은 시간이 지남에 따라 비선형 PK를 나타냅니다. 세리티닙의 기하 평균 명백 청소율(CL/F)은 750mg을 1일 투여한 후 정상 상태(33.2L/h)에서 750mg을 단회 투여한 후(88.5L/h)보다 낮았습니다.
대사: in vitro 연구 결과 CYP3A가 세리티닙의 대사 청소율에 관여하는 주요 효소임을 밝혀냈습니다. 금식 상태에서 방사성 동위원소 표지된 750mg을 단회 경구 투여한 후, 세리티닙은 인간 혈장에서 주요 순환 성분(82%)이었습니다.
배설: 금식 상태에서 방사성 동위원소 표지된 750mg을 단회 경구 투여한 후, 투여된 용량의 92%가 대변에서 회수되었으며(변경되지 않은 모 화합물 68% 포함) 투여된 용량의 1.3%가 소변에서 회수되었습니다.
특정 인구 집단
인구 약동학 분석 결과, 연령, 성별, 인종, 체중 및 경증에서 중등도 신장애(Cockcroft-Gault로 추정한 CLcr 30~< 90mL/min)는 세리티닙의 전신 노출에 임상적으로 중요한 영향을 미치지 않습니다. 중증 신장애(CLcr < 30mL/min) 환자는 임상 시험에 포함되지 않았습니다.
간 기능 장애 환자: 금식 상태에서 단일 750mg ZYKADIA 용량을 투여한 후, 중증 (Child-Pugh C) 간 기능 장애 환자에서 정상 간 기능 환자에 비해 세리티닙의 기하 평균 전신 노출 (AUC0-INF)이 66% 증가하고 비결합 세리티닙 AUC0-INF가 108% 증가했습니다 [용법 및 용량 (2.5) 참조]. 세리티닙의 총 전신 노출 및 비결합 전신 노출은 경증 (Child-Pugh A)에서 중등도 (Child-Pugh B) 간 기능 장애 환자에서 정상 간 기능 환자와 유사했습니다.
약물 상호 작용 연구
세리티닙에 대한 강력한 CYP3A/P-gp 억제제의 영향: 금식 상태에서 단일 450mg ZYKADIA 용량을 14일 동안 케토코나졸 (강력한 CYP3A/P-gp 억제제)과 함께 투여하면 세리티닙 AUC가 2.9배 증가하고 Cmax가 22% 증가했습니다. 케토코나졸과 함께 14일 동안 금식 상태에서 1일 1회 450mg 용량으로 투여한 세리티닙의 정상 상태 AUC는 금식 상태에서 750mg 단독으로 투여한 세리티닙의 정상 상태 AUC와 유사할 것으로 예상됩니다.
세리티닙에 대한 강력한 CYP3A/P-gp 유도제의 영향: 금식 상태에서 단일 750mg ZYKADIA 용량을 14일 동안 리팜핀 (강력한 CYP3A/P-gp 유도제)과 함께 투여하면 세리티닙 AUC가 70% 감소하고 Cmax가 44% 감소했습니다.
CYP3A 기질에 대한 세리티닙의 영향: 금식 상태에서 3주 동안 ZYKADIA (1일 750mg)를 투여한 후 단일 용량의 미다졸람 (민감한 CYP3A 기질)을 함께 투여하면 미다졸람 AUC가 5.4배 증가하고 Cmax가 1.8배 증가했습니다. 미다졸람을 단독으로 투여한 경우와 비교했습니다 [약물 상호 작용 (7.2) 참조].
CYP2C9 기질에 대한 세리티닙의 영향: 금식 상태에서 3주 동안 ZYKADIA (1일 750mg)를 투여한 후 단일 용량의 와파린 (CYP2C9 기질)을 함께 투여하면 S-와파린 AUC가 54% 증가했지만 Cmax는 와파린을 단독으로 투여한 경우와 비교하여 변화가 없었습니다 [약물 상호 작용 (7.2) 참조].
산 감소제에 대한 세리티닙의 영향: 건강한 피험자에서 금식 상태에서 단일 750mg ZYKADIA 용량을 6일 동안 프로톤 펌프 억제제 (에소메프라졸)와 함께 투여하면 세리티닙 AUC가 76% 감소하고 Cmax가 79% 감소했습니다. 그러나 ASCEND-1의 환자 하위 그룹에서 금식 상태에서 단일 750mg ZYKADIA 용량을 6일 동안 프로톤 펌프 억제제와 함께 투여하면 건강한 피험자에서 관찰된 것보다 세리티닙 노출에 대한 영향이 적은 것으로 나타났습니다. AUC는 30% 감소하고 Cmax는 25% 감소했으며 정상 상태에서 세리티닙 노출에 대한 임상적으로 의미 있는 영향은 관찰되지 않았습니다.
세리티닙 배설에 대한 수송체의 영향: 세리티닙은 유출 수송체 P-gp의 기질이지만, 시험관 내에서 BCRP, MRP2, OCT1, OAT2 또는 OATP1B1의 기질이 아닙니다.
수송체에 대한 세리티닙의 영향: 시험관 내 데이터를 기반으로, 세리티닙은 임상 농도에서 P-gp, BCRP, MRP2, OATP1B1, OATP1B3, OAT1, OAT3, OCT1 또는 OCT2를 억제할 가능성이 낮습니다.
13 비임상 독성학
13.1
발암성, 돌연변이 유발성, 생식능력 손상
세리티닙을 사용한 발암성 연구는 수행된 바 없습니다.
세리티닙은 박테리아 역돌연변이(Ames) 분석에서 시험관내 돌연변이 유발성을 나타내지 않았지만, 인간 림프구를 사용한 시험관내 세포유전학적 분석에서 수적 이상(이수성)을 유발했으며, TK6 세포를 사용한 시험관내 소핵 시험에서 소핵을 유발했습니다. 세리티닙은 생체내 랫트 소핵 분석에서 염색체 절단성을 나타내지 않았습니다.
세리티닙이 인간 생식능력에 미치는 영향에 대한 데이터는 없습니다. 세리티닙을 사용한 생식능력/초기 배아 발생 연구는 수행된 바 없습니다. 권장 용량에서 AUC 기준으로 사람에게 노출되는 양의 ≥ 0.5배 및 1.5배에 노출된 원숭이와 랫트를 대상으로 실시한 일반 독성학 연구에서 수컷 또는 암컷 생식 기관에 대한 부작용은 관찰되지 않았습니다.
13.2
동물 독성학 및/또는 약리학
비임상 동물 모델에서 표적 장기에는 췌장, 췌담도/담도, 위장관, 간이 포함되었지만 이에 국한되지는 않았습니다. 췌장의 초점성 선방 세포 위축은 권장 용량에서 AUC 기준으로 사람에게 노출되는 양의 1.5배에 노출된 랫트에서 관찰되었습니다. 췌담도 및 담도 괴사는 권장 용량에서 AUC 기준으로 사람에게 노출되는 양의 ≥ 5%에 노출된 랫트에서 관찰되었습니다. 담도 염증 및 공포화는 또한 권장 용량에서 AUC 기준으로 사람에게 노출되는 양의 ≥ 0.5배에 노출된 원숭이에서도 나타났습니다. 십이지장의 빈번한 최소 괴사 및 출혈은 AUC 기준으로 사람에게 노출되는 양의 0.5배에 노출된 원숭이와 임상적으로 관찰된 것과 유사한 노출 수준의 랫트에서 나타났습니다.
세리티닙은 약 15%의 뇌-혈액 노출(AUCinf) 비율로 랫트의 혈액뇌장벽을 통과했습니다.
14 임상 연구
14.1
ALK 양성 전이성 비소세포폐암 치료를 받지 않은 환자
전이성 질환에 대한 이전 전신 치료를 받지 않은 ALK 양성 NSCLC 환자의 ZYKADIA 치료 효능은 개방형, 무작위 배정, 활성 대조, 다기관 연구(ASCEND-4, NCT01828099)에서 평가되었습니다. 환자는 세계보건기구(WHO) 기능 상태 0-2 및 VENTANA ALK(D5F3) CDx 검사에서 확인된 ALK 양성 NSCLC를 가져야 했습니다. 중추신경계(CNS) 증상 관리를 위해 스테로이드 용량 증가가 필요하지 않은 중추신경계 전이가 있는 신경학적으로 안정적인 환자는 등록이 허용되었습니다. 통제되지 않은 당뇨병; ILD 또는 간질성 폐렴의 병력; 또는 췌장 질환으로 인한 췌장염 또는 아밀라아제 또는 리파아제 증가의 병력이 있는 환자는 적격하지 않았습니다.
주요 효능 결과 측정은 RECIST v1.1에 따라 눈가림 독립 검토 위원회(BIRC)가 결정한 무진행 생존(PFS)이었습니다. 추가 효능 결과 측정은 BIRC가 결정한 전체 생존(OS), 전체 반응률(ORR) 및 반응 지속 기간(DOR), BIRC 신경 방사선과 의사가 결정한 전체 두개내 반응률(OIRR), 두개내 반응 지속 기간(DOIR) 및 환자 보고 결과였습니다.
환자는 1:1로 무작위 배정되어 금식 상태에서 경구로 ZYKADIA 750mg을 매일 투여받거나 화학 요법 및 유지 화학 요법을 받았습니다. 무작위 배정은 WHO 기능 상태, 이전 보조/신보조 화학 요법 및 뇌 전이 유무에 따라 계층화되었습니다. 화학 요법에 무작위 배정된 환자는 21일 주기의 1일에 최대 4주기 동안 페메트렉세드(500mg/m2)와 연구자의 선택에 따라 시스플라틴(75mg/m2) 또는 카보플라틴(AUC 5-6mg*min/mL)을 투여받았으며, 이후 21일마다 페메트렉세드(500mg/m2)를 투여받았습니다. 두 군 모두에서 치료는 질병 진행 또는 용납할 수 없는 독성이 나타날 때까지 계속되었습니다.
연구 모집단 특징은 다음과 같습니다. 여성 57%, 중앙값 연령 54세(범위 22~81세), 65세 이상 22%, 백인 54%, 아시아인 42%, 흑인 2%, 기타 인종 2%. 대부분의 환자는 선암(97%)이었고, 담배를 피운 적이 없었습니다(61%). CNS 전이는 환자의 32%(n=121)에서 나타났습니다. BIRC 신경 방사선과 의사가 결정한 측정 가능한 CNS 전이는 약 절반(n=55)에서 나타났으며, 이러한 환자 중 71%(n=39)는 이전에 두개내 방사선 치료를 받지 않았습니다. 화학 요법에 무작위 배정된 환자 중 43%는 백금 기반 화학 요법 후 다음 항암 치료로 ZYKADIA를 받았습니다.
ASCEND-4의 효능 결과는 표 7과 그림 1에 요약되어 있습니다.
| 효능 매개변수 | ZYKADIA (N = 189) |
화학 요법 (N = 187) |
| 무진행 생존 | ||
| 사건 수, n (%) | 89 (47%) | 113 (60%) |
| 진행성 질환, n (%) | 79 (42%) | 105 (56%) |
| 사망, n (%) | 10 (5%) | 8 (4%) |
| 중앙값 PFS(월)(95% CI) | 16.6 (12.6, 27.2) | 8.1 (5.8, 11.1) |
| 위험 비율(95% CI)a | 0.55 (0.42, 0.73) | |
| P 값b | < 0.0001 | |
| 전체 반응률 | ||
| 전체 반응률, %(95% CI)c | 73 (66, 79) | 27 (21, 34) |
| 완전 반응, % | 1 | 0 |
| 부분 반응, % | 72 | 27 |
| 반응 지속 기간 | ||
| 반응자 수 | n = 137 | n = 50 |
| 중앙값(월)(95% CI) | 23.9 (16.6, NE) | 11.1 (7.8, 16.4) |
| 약어: BIRC, 눈가림 독립 검토 위원회; CI, 신뢰 구간; NE, 추정 불가. a뇌 전이(없음 대 비해 있음), WHO 기능 상태(0 대 비해 ≥ 1), 이전 보조 화학 요법(없음 대 비해 있음)에 따라 계층화된 Cox 비례 위험 모델. b뇌 전이(없음 대 비해 있음), WHO 기능 상태(0 대 비해 ≥ 1), 이전 보조 화학 요법(없음 대 비해 있음)에 따라 계층화된 로그 순위 검정. cClopper 및 Pearson 정확 이항 95% CI. |
||
최종 분석에 필요한 사건의 42%에서 실시된 사전 지정된 중간 분석에서 OS에 유의미한 차이가 없었습니다.
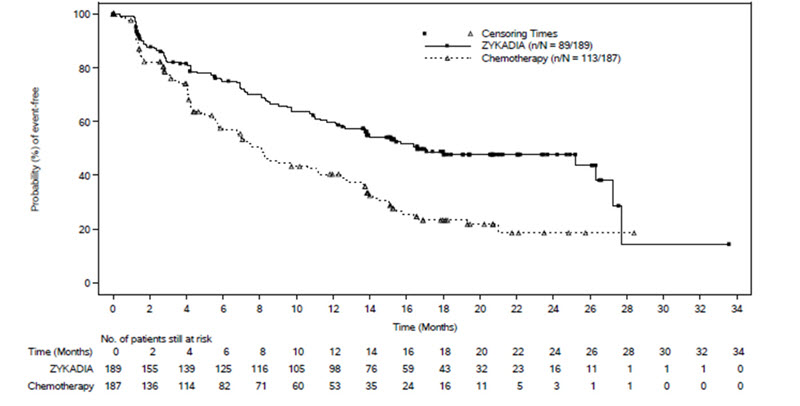
그림 1: ASCEND-4에서 치료군별 BIRC에 의해 평가된 무진행 생존의 Kaplan-Meier 플롯
ZYKADIA의 뇌에서의 항종양 활성은 기준선에서 BIRC 신경 방사선과에 의해 측정 가능한 질환으로 판정된 환자(N = 55)에서 RECIST 1.1에 따라 평가되었습니다.
| 두개내 종양 반응 평가 | ZYKADIA (N = 28) |
화학 요법 (N = 27) |
| 전반적인 두개내 반응률, %(95% CI)a |
57% (37, 76) |
22% (9, 42) |
| 완전 반응, % | 7% | 7% |
| 부분 반응, % | 50% | 15% |
| 두개내 반응 지속 기간 | ||
| 반응자 수 | n = 16 | n = 6 |
| 중앙값(월)(95% CI) | 16.6 (8.1, NE) | NE (1.5, NE) |
| 약어: BIRC, 맹검 독립 검토 위원회; CI, 신뢰 구간; CNS, 중추 신경계; NE, 추정 불가. aClopper 및 Pearson 정확한 이항 95% CI. |
||
환자 보고 결과 측정치에 대한 탐색적 분석은 ZYKADIA로 치료받은 환자에서 화학 요법과 비교하여 호흡 곤란의 발생 또는 악화까지의 시간이 지연됨을 시사했습니다. 환자 보고된 호흡 곤란의 발생 또는 악화 지연은 환자가 치료 배정에 대해 맹검되지 않았기 때문에 과대 평가일 수 있습니다.
14.2
이전에 치료받은 ALK 양성 전이성 NSCLC
ZYKADIA의 효능은 다기관, 단일군, 공개 표지 임상 시험(ASCEND-1, NCT01283516)에서 평가되었습니다. 크리조티닙을 투여받는 동안 진행되었거나 크리조티닙에 내성이 있는 전이성 ALK 양성 NSCLC 환자 163명이 등록되었습니다. 주요 효능 결과 측정치는 연구자와 BIRC 모두에 의해 평가된 RECIST v1.0에 따른 객관적 반응률(ORR)이었습니다. 반응 지속 기간은 추가 결과 측정치였습니다. 모든 환자는 금식 상태에서 1일 1회 750mg의 ZYKADIA를 투여받았습니다.
연구 대상 환자 특징은 다음과 같습니다. 중앙값 연령 52세, 65세 미만 연령(87%), 여성(54%), 백인(66%), 아시아인(29%), 비흡연자 또는 과거 흡연자(97%), ECOG PS 0 또는 1(87%), 이전 크리조티닙에 대한 진행(91%), 이전 치료 횟수 2회 이상(84%), 그리고 선암 조직학(93%). 흉곽 외 전이 부위에는 뇌(60%), 간(42%), 뼈(42%)가 포함되었습니다. ALK 양성은 환자의 99%에 대해 지역 검사 결과를 검토하여 역행적으로 확인되었습니다.
ASCEND-1의 효능 결과는 표 9에 요약되어 있습니다.
| 효능 매개변수 | 연구자 평가 (N = 163) |
BIRC 평가 (N = 163) |
| 전체 반응률, % (95% CI) |
55% (47, 62) |
44% (36, 52) |
| 완전 반응, % | 1.2% | 2.5% |
| 부분 반응, % | 53% | 41% |
| 반응 지속 기간, 중앙값(월) (95% CI) |
7.4 (5.4, 10.1) |
7.1 (5.6, NE) |
| 약어: BIRC, 맹검 독립 검토 위원회; CI, 신뢰 구간; NE, 추정 불가. 1RECIST v1.0에 의해 결정된 전체 반응률 및 반응 지속 기간. |
||
BIRC 평가에 의한 분석은 연구자 평가에 의한 분석과 유사했습니다.
16 제공/보관 및 취급 방법
ZYKADIA 150 mg 캡슐
불투명한 파란색 캡과 불투명한 흰색 바디가 있는 경질 젤라틴 캡슐; 불투명한 파란색 캡은 검은색 잉크로 “LDK 150MG”로 표시되고, 불투명한 흰색 바디는 검은색 잉크로 “NVR”로 표시됩니다. 다음과 같이 제공됩니다.
70 캡슐 병…………………………………………………………………………………….NDC 0078-0640-70
20°C~25°C(68°F~77°F)에 보관하십시오. 15°C~30°C(59°F~86°F)의 변동은 허용됩니다. [USP 제어 실온 참조]
ZYKADIA 150 mg 정제
엷은 파란색, 둥근, 양쪽 볼록, 경사가 있는 가장자리, 쪼개짐 없이, 한쪽에는 “NVR”, 다른 쪽에는 “ZY1”이 각인된 필름 코팅 정제. 다음과 같이 제공됩니다.
84 정제 병…………………………………………………………………………………NDC 0078-0694-84
20°C~25°C(68°F~77°F)에 보관하십시오. 15°C~30°C(59°F~86°F)의 변동은 허용됩니다. [USP 제어 실온 참조]
17 환자 상담 정보
환자에게 FDA 승인을 받은 환자 라벨링(환자 정보)을 읽도록 권고하십시오.
위장관계 이상반응
환자에게 설사, 메스꺼움, 구토 및 복통이 가장 흔하게 보고되는 위장관계 이상반응임을 알리십시오. 구토 억제제 및 지사제와 같은 지지 요법에 대해 환자에게 알리십시오. 심각하거나 참을 수 없는 위장관 증상이 나타나면 의료 서비스 제공자에게 연락하도록 환자에게 조언하십시오. 치료 과정 중 구토가 발생하면 추가 용량을 복용하지 않고 예정된 다음 ZYKADIA 용량을 계속 복용해야 함을 환자에게 알리십시오. [경고 및 주의사항(5.1) 참조].
간독성
환자에게 간독성의 징후와 증상을 알리십시오. 간독성의 징후나 증상이 나타나면 즉시 의료 서비스 제공자에게 연락하도록 환자에게 조언하십시오. [경고 및 주의사항(5.2) 참조].
Interstitial Lung Disease/Pneumonitis
심각하거나 치명적인 ILD/폐렴의 위험에 대해 환자에게 알리십시오. 새로운 호흡기 증상이나 악화되는 호흡기 증상을 보고하려면 즉시 의료 서비스 제공자에게 연락하도록 환자에게 조언하십시오. [경고 및 주의사항(5.3) 참조].
Arrhythmias
QTc 간격 연장 및 서맥의 위험에 대해 환자에게 알리십시오. 새로운 흉통이나 불편함, 심장 박동 변화, 심계항진, 현기증, 어지러움, 실신, 심장 또는 혈압 약물의 사용 변화 또는 새로운 사용을 보고하려면 즉시 의료 서비스 제공자에게 연락하도록 환자에게 조언하십시오. [경고 및 주의사항(5.4, 5.6) 참조].
고혈당증
환자에게 고혈당증의 징후와 증상을 알리십시오. 고혈당증의 징후나 증상이 나타나면 즉시 의료 서비스 제공자에게 연락하도록 환자에게 조언하십시오. [경고 및 주의사항(5.5) 참조].
췌장염
환자에게 췌장염의 징후와 증상, 그리고 치료 시작 전과 그 이후 임상적으로 필요에 따라 주기적으로 리파아제 및 아밀라아제 수치를 모니터링해야 할 필요성을 알리십시오. [경고 및 주의사항(5.7) 참조].
광과민성
환자에게 광과민성의 징후와 증상을 알리십시오. ZYKADIA 치료 중에는 장시간 햇볕에 노출되지 않도록 하고 자외선 차단제나 보호복을 착용하도록 환자에게 조언하십시오. [이상반응(6.1) 참조].
태아 독성
- 임산부와 가임 여성에게 태아에 대한 잠재적 위험을 알리고 알려진 임신이나 의심되는 임신을 의료 서비스 제공자에게 알리도록 조언하십시오. [경고 및 주의사항(5.8), 특정 집단에서의 사용(8.3) 참조].
- 가임 여성에게 ZYKADIA 치료 중 및 치료 완료 후 6개월 동안 효과적인 피임법을 사용하도록 조언하십시오. [특정 집단에서의 사용(8.3) 참조].
- 가임 여성 파트너가 있는 남성에게 ZYKADIA 치료 중 및 치료 완료 후 3개월 동안 콘돔을 사용하도록 조언하십시오. [특정 집단에서의 사용(8.3), 비임상 독성학(13.1) 참조].
수유
여성에게 ZYKADIA 치료 중 및 치료 완료 후 2주 동안 모유 수유를 하지 않도록 조언하십시오. [특정 집단에서의 사용(8.2) 참조].
약물 상호 작용
환자에게 ZYKADIA 치료 중 자몽과 자몽 주스를 섭취하지 않도록 알리십시오. [약물 상호 작용(7.1) 참조].
복용 지침
환자에게 ZYKADIA를 음식과 함께 복용하도록 조언하십시오. [용량 및 투여(2.2) 참조]. 다음 복용 시간까지 12시간 이내인 경우를 제외하고 ZYKADIA 복용을 잊은 경우 복용하도록 환자에게 조언하십시오. [용량 및 투여(2.2) 참조].
Distributed by:
Novartis Pharmaceuticals Corporation
East Hanover, New Jersey 07936
© Novartis
T2021-132
환자 안내문
| 이 환자 정보는 미국 식품의약국(FDA)에 의해 승인되었습니다. | 개정: 2021년 10월 | ||||
| 환자 정보 ZYKADIA® (지케이디아) (세리티닙) 캡슐 (세리티닙) 정제 |
|||||
| ZYKADIA를 복용하기 전과 매번 재채움을 받을 때마다 함께 제공되는 이 환자 정보 전단지를 읽으십시오. 새로운 정보가 있을 수 있습니다. 이 정보는 의료 상태 또는 치료에 관해 의료진과의 상담을 대신하지 않습니다. | |||||
| ZYKADIA에 관해서 가장 중요한 정보는 무엇인가요? ZYKADIA는 심각한 부작용을 일으킬 수 있으며, 이에는 다음이 포함됩니다: 위장 및 장(위장관) 문제. ZYKADIA는 설사, 메스꺼움, 구토, 복부 통증 등의 위장 및 장 문제를 유발할 수 있습니다. 이러한 증상에 도움이 되는 약물 복용에 관한 의료진의 지시를 따르십시오. 증상이 심하거나 견디기 어려운 경우 의료진에게 조언을 구하십시오. 간 문제. ZYKADIA는 간 손상을 일으킬 수 있습니다. 의료진은 ZYKADIA 치료 동안 적어도 매달 혈액 검사를 통해 간을 검사해야 합니다. 다음과 같은 증상이 있으면 즉시 의료진에게 말씀하십시오: |
|||||
| • 피곤함을 느끼는 경우 | • 피부가 가려운 경우 | ||||
| • 피부 또는 눈의 흰자위가 노랗게 변하는 경우 | • 메스꺼움 또는 구토가 있는 경우 | ||||
| • 식욕이 감소하는 경우 | • 복부 오른쪽에 통증이 있는 경우 | ||||
| • 소변의 색이 어둡거나 갈색(홍차색)으로 변하는 경우 | • 쉽게 출혈하거나 멍이 드는 경우 | ||||
| 폐 문제(폐렴). ZYKADIA는 치료 중에 심각하거나 생명을 위협하는 폐의 염증을 유발하여 사망에 이를 수 있습니다. 증상은 폐암의 증상과 유사할 수 있습니다. 다음과 같은 새로운 또는 악화된 증상이 있으면 즉시 의료진에게 말씀하십시오, 이에는: | |||||
| • 호흡 곤란 또는 숨이 차는 경우 | • 가래가 있거나 없는 기침 | ||||
| • 발열 | • 흉통 | ||||
| 심장 문제. ZYKADIA는 매우 느리거나 매우 빠르거나 비정상적인 심장 박동을 유발할 수 있습니다. 의료진은 ZYKADIA 치료 중에 심장을 검사할 수 있습니다. 새로운 가슴 통증 또는 불편함, 현기증 또는 어지러움, 실신하거나 비정상적인 심장 박동을 느끼면 즉시 의료진에게 말씀하십시오. 심장 또는 혈압 약물을 시작하거나 변경하는 경우에도 의료진에게 말씀하십시오. “ZYKADIA의 가능한 부작용은 무엇인가요?”에서 부작용에 대한 더 많은 정보를 확인하십시오. |
|||||
| ZYKADIA는 무엇인가요? ZYKADIA는 다음과 같은 비소세포폐암(NSCLC) 환자를 치료하는 데 사용되는 처방약입니다:
ZYKADIA가 어린이에게 안전하고 효과적인지 알려지지 않았습니다. |
|||||
ZYKADIA를 복용하기 전에, 다음과 같은 모든 의료 상태에 대해 의료진에게 말씀하십시오, 이에는:
복용하고 있는 모든 약물, 이에는 처방약, 비처방약, 비타민 및 허브 보충제를 의료진에게 말씀하십시오. |
|||||
ZYKADIA를 어떻게 복용해야 하나요?
|
|||||
ZYKADIA 복용 시 피해야 할 것은 무엇입니까?
|
|||||
| ZYKADIA의 가능한 부작용은 무엇입니까? ZYKADIA는 다음을 포함한 심각한 부작용을 일으킬 수 있습니다.
|
|||||
| • 갈증 증가 | • 배고픔 증가 | • 두통 | • 생각하거나 집중하는 데 어려움 | ||
| • 잦은 배뇨 | • 시야 흐림 | • 피로 | • 숨에서 과일 냄새가 남 | ||
ZYKADIA의 가장 흔한 부작용은 다음과 같습니다.
이것들이 ZYKADIA의 가능한 모든 부작용은 아닙니다. 자세한 내용은 담당 의료 제공자 또는 약사에게 문의하십시오. 부작용에 대한 의학적 조언은 의사에게 문의하십시오. 1-800-FDA-1088로 FDA에 부작용을 보고할 수 있습니다. |
|||||
ZYKADIA는 어떻게 보관해야 합니까?
ZYKADIA 및 모든 의약품은 어린이의 손이 닿지 않는 곳에 보관하십시오. |
|||||
| ZYKADIA의 안전하고 효과적인 사용에 대한 일반 정보 의약품은 때때로 환자 정보 전단지에 나열된 것 이외의 목적으로 처방되기도 합니다. 처방되지 않은 질환에 ZYKADIA를 사용하지 마십시오. 같은 증상이 있더라도 다른 사람에게 주지 마십시오. 그들에게 해를 끼칠 수 있습니다. 담당 의료 제공자 또는 약사에게 의료 전문가를 위해 작성된 ZYKADIA에 대한 자세한 정보를 요청할 수 있습니다. |
|||||
| ZYKADIA의 성분은 무엇입니까? 활성 성분: ceritinib 캡슐의 비활성 성분: 콜로이드성 이산화규소, 경질 젤라틴 캡슐 껍질, 저치환도 히드록시프로필 셀룰로오스, 스테아르산마그네슘, 미결정셀룰로오스, 글리콜산나트륨전분. 캡슐 껍질에는 FD&C 블루 #2, 젤라틴, 이산화티타늄이 포함되어 있습니다. 정제의 비활성 성분: 정제 코어: 콜로이드성 이산화규소, 크로스카르멜로스나트륨, 저치환도 히드록시프로필 셀룰로오스, 스테아르산마그네슘, 미결정셀룰로오스, 포비돈. 정제 코팅: FD&C 블루 #2 알루미늄 레이크, 히프로멜로스, 폴리에틸렌글리콜 4000, 탈크, 이산화티타늄. 유통: Novartis Pharmaceuticals Corporation, East Hanover, New Jersey 07936. 자세한 내용은 www.US.ZYKADIA.com을 방문하거나 1-888-669-6682로 전화하십시오. |
|||||
T2021-133
주요 디스플레이 패널
NDC 0078-0694-84
Zykadia®
(ceritinib) 정제
150 mg
84정
처방전 필요
NOVARTIS


